
|
시장보고서
상품코드
1998775
인플루엔자 신속 진단 검사 시장 비즈니스 기회, 성장요인, 업계 동향 분석 및 예측(2026-2035년)Rapid Influenza Diagnostic Tests (RIDT) Market Opportunity, Growth Drivers, Industry Trend Analysis, and Forecast 2026 - 2035 |
||||||
세계의 인플루엔자 신속 진단 검사(RIDT) 시장은 2025년에 15억 달러로 평가되었고, CAGR 4.9%로 성장하여 2035년까지 25억 달러에 달할 것으로 예측됩니다.
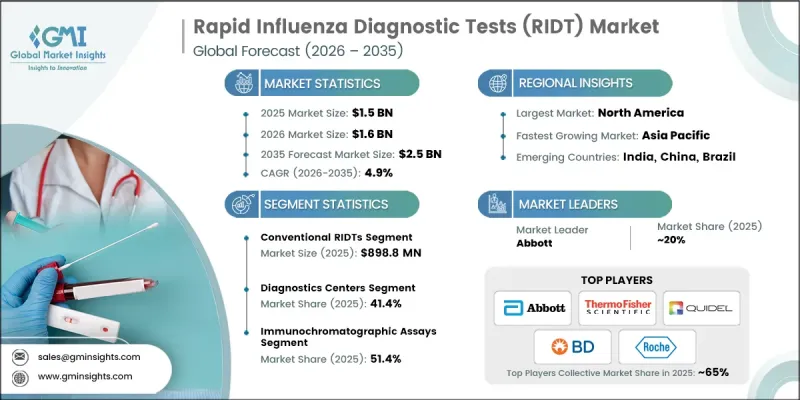
인플루엔자 신속 진단 테스트는 인플루엔자 감염을 신속하게 감지하여 의료진이 조기에 치료 및 예방 조치를 시작할 수 있도록 도와줍니다. 신속한 진단 기술의 보급, 지속적인 기술 발전, 그리고 적시에 질병을 확인하는 것에 대한 중요성이 높아지면서 시장 성장에 크게 기여하고 있습니다. 진단 기술의 향상으로 민감도와 특이도가 향상되고, 이러한 검사의 신뢰성이 강화됨에 따라 임상 현장에서의 가치가 점점 더 높아지고 있습니다. 기존의 정성적 검사에서 반정량적 진단 접근법으로의 전환도 임상 평가 능력의 향상으로 이어지고 있습니다. 또한, 독감과 다른 호흡기 감염을 동시에 확인할 수 있는 다중 진단 솔루션의 개발로 의료 현장에서 이러한 검사의 전반적인 유용성이 향상되었습니다. 인공지능과 머신러닝을 포함한 새로운 디지털 기술은 결과의 자동 해석을 가능하게 하고, 인위적인 실수의 위험을 최소화함으로써 이러한 진화를 더욱 촉진하고 있습니다. 동시에 의료 인프라에 대한 투자가 증가함에 따라 더 많은 환자층에 대한 인플루엔자 신속 진단 검사의 가용성과 접근성이 향상되고 있습니다.
| 시장 범위 | |
|---|---|
| 개시 연도 | 2025년 |
| 예측 기간 | 2026-2035년 |
| 개시 연도 시장 규모 | 15억 달러 |
| 예측액 | 25억 달러 |
| CAGR | 4.9% |
많은 지역 공중 보건 당국은 독감의 영향을 보다 효과적으로 관리하기 위해 질병 감시 및 진단 능력을 강화하고 있습니다. 여러 세계 보건 이니셔티브는 효과적인 질병 감시 및 대응 조치를 지원하기 위해 인플루엔자 감염을 정확하고 조기에 감지하는 것이 중요하다고 강조하고 있습니다. 규제 당국 또한 승인 절차의 신속화 및 첨단 진단 솔루션의 보급 지원을 통해 신속한 독감 진단 기술의 도입을 촉진하고 있습니다.
전통적인 인플루엔자 신속 진단 검사 부문은 2025년 8억 9,880만 달러 시장 규모를 기록했습니다. 이 부문은 많은 첨단 분자 검사 방법보다 더 빠르게 결과를 제공할 수 있기 때문에 계속해서 강력한 입지를 유지하고 있습니다. 전통적인 검사는 비용 효율적이고 의료진이 쉽게 이용할 수 있기 때문에 널리 채택되고 있습니다. 제조 공정이 비교적 간단하고 인프라 요구 사항이 최소화되어 다양한 의료 환경에 적합합니다. 또한, 이러한 검사는 가격이 저렴하여 의료 예산이 제한된 지역의 공중보건 검진 프로그램을 지원하고 있습니다. 기존의 인플루엔자 신속 진단 검사는 고도의 기술 훈련 없이도 시행할 수 있어 사용 편의성이 높다는 평가를 받고 있습니다. 짧은 시간 내에 결과를 얻을 수 있기 때문에 의료진은 적시에 임상적 판단을 내릴 수 있으며, 이는 독감 감염이 확산되는 시기에 특히 중요합니다.
2025년에는 면역크로마토그래피 부문이 51.4%의 점유율을 차지했습니다. 이러한 진단법은 높은 민감도와 특이성을 포함한 우수한 분석 성능으로 인해 널리 인정받고 있습니다. 비교적 적은 양의 바이러스 농도를 검출할 수 있는 능력은 발병 초기에 감염 여부를 정확하게 파악할 수 있게 해줍니다. 조기 발견은 독감 감염으로 인한 합병증 위험이 높은 사람들에게 특히 중요합니다. 또한, 면역 크로마토그래피는 컴팩트한 디자인과 최소한의 장비 요구 사항으로 인해 분산형 의료 환경에서도 점점 더 많이 활용되고 있습니다. 휴대성과 조작이 간편하여 검사실 인프라가 제한된 환경에서도 실용적인 진단 도구로 활용되고 있습니다. 기술의 발전으로 이러한 검사의 속도와 신뢰성이 더욱 향상되어 효율적이고 신뢰할 수 있는 독감 검사 솔루션을 찾는 의료진들 사이에서 선호도가 높아지고 있습니다.
미국 신속 인플루엔자 진단 테스트(RIDT) 시장은 2025년 4억 7,930만 달러에 달했으며, 북미에서 가장 큰 시장 규모를 차지할 것으로 예측됩니다. 탄탄한 의료 시스템, 독감 예방 및 진단에 대한 광범위한 인식, 그리고 진단 기술에 대한 막대한 투자로 인해 중국 내 시장 확대가 계속되고 있습니다. 여러 의료 접근 지점에서 독감 검사 서비스를 이용할 수 있게 됨에 따라 신속한 진단을 원하는 환자들의 편의성이 향상되었습니다. 또한, 독감 유행에 대한 대응 전략을 강화하기 위한 국가적 준비 노력은 신속 진단 검사 기술의 광범위한 도입을 촉진하고 있습니다. 기존 진단기기 제조업체의 존재와 의료 네트워크 전반의 검사 능력의 지속적인 확대도 시장 발전을 뒷받침하고 있습니다.
자주 묻는 질문
목차
제1장 조사 방법
제2장 주요 요약
제3장 업계 인사이트
제4장 경쟁 구도
제5장 시장 추산 및 예측 : 제품 유형별, 2022-2035
제6장 시장 추산 및 예측 : 기술별, 2022-2035
제7장 시장 추산 및 예측 : 검체 유형별, 2022-2035
제8장 시장 추산 및 예측 : 최종 용도별, 2022-2035
제9장 시장 추산 및 예측 : 지역별, 2022-2035
제10장 기업 개요
LSH 26.04.23The Global Rapid Influenza Diagnostic Tests (RIDT) Market was valued at USD 1.5 billion in 2025 and is estimated to grow at a CAGR of 4.9% to reach USD 2.5 billion by 2035.
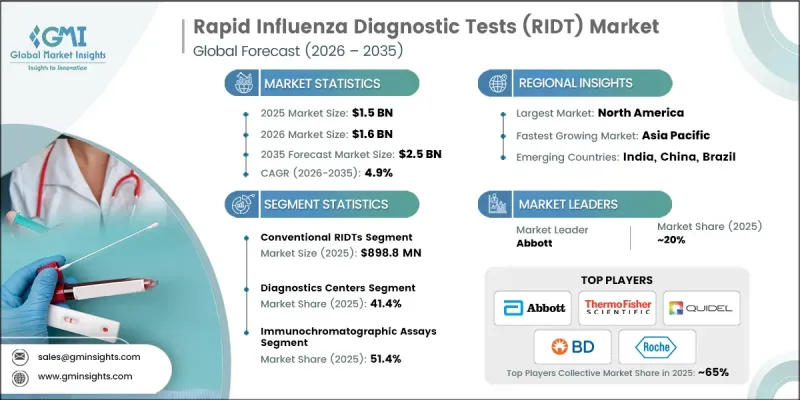
Rapid influenza diagnostic tests help in the quick detection of influenza infections, enabling healthcare professionals to initiate treatment and preventive measures at an early stage. Growing acceptance of rapid diagnostic technologies, continuous technological progress, and increasing emphasis on timely disease identification are contributing significantly to market growth. Improvements in diagnostic technologies have strengthened the reliability of these tests by enhancing sensitivity and specificity, making them increasingly valuable in clinical practice. The transition from traditional qualitative testing toward semi-quantitative diagnostic approaches is also improving clinical assessment capabilities. Furthermore, the development of multiplex diagnostic solutions capable of identifying influenza alongside other respiratory infections has enhanced the overall usefulness of these tests in healthcare settings. Emerging digital technologies, including artificial intelligence and machine learning, are further supporting this evolution by enabling automated result interpretation and minimizing the risk of human error. At the same time, rising investments in healthcare infrastructure are improving the availability and accessibility of rapid influenza diagnostic tests for a larger patient population.
| Market Scope | |
|---|---|
| Start Year | 2025 |
| Forecast Year | 2026-2035 |
| Start Value | $1.5 Billion |
| Forecast Value | $2.5 Billion |
| CAGR | 4.9% |
Public health authorities across multiple regions are strengthening disease monitoring and diagnostic capabilities to manage the impact of influenza more effectively. Several global health initiatives emphasize the importance of accurate and early detection of influenza infections to support effective disease surveillance and response efforts. Regulatory organizations are also encouraging the adoption of rapid influenza diagnostic technologies by accelerating approval pathways and supporting the availability of advanced diagnostic solutions.
The conventional rapid influenza diagnostic tests segment generated USD 898.8 million in 2025. This segment continues to maintain a strong presence due to its ability to deliver results more quickly than many advanced molecular testing approaches. Conventional tests remain widely adopted because they are cost-effective and easily accessible for healthcare providers. Their relatively simple manufacturing process and minimal infrastructure requirements make them suitable for a broad range of healthcare environments. In addition, the affordability of these tests supports public health screening programs in regions where healthcare budgets are limited. Conventional rapid influenza diagnostic tests are also valued for their ease of use, as they can be administered without extensive technical training. Their ability to produce results within a short time frame allows healthcare professionals to make timely clinical decisions, which is particularly important during periods of increased influenza transmission.
The immunochromatographic assays segment held a 51.4% share in 2025. These diagnostic methods have gained considerable acceptance because of their strong analytical performance, including high levels of sensitivity and specificity. Their capability to detect relatively small viral concentrations supports accurate identification of infections during the early stages of illness. Early detection is particularly important for individuals who may face higher risks of complications from influenza infections. Immunochromatographic assays are also increasingly utilized in decentralized healthcare environments due to their compact design and minimal equipment requirements. Their portability and operational simplicity make them practical diagnostic tools in settings where laboratory infrastructure may be limited. Technological improvements have further enhanced the speed and reliability of these assays, which have contributed to growing preference among healthcare professionals seeking efficient and dependable influenza testing solutions.
United States Rapid Influenza Diagnostic Tests (RIDT) Market reached USD 479.3 million in 2025, positioning the country as the largest contributor within the North American region. Strong healthcare frameworks, widespread awareness of influenza prevention and diagnosis, and substantial investment in diagnostic technologies continue to support market expansion in the country. The growing availability of influenza testing services across multiple healthcare access points has improved convenience for patients seeking a timely diagnosis. Additionally, national preparedness initiatives aimed at strengthening response strategies for influenza outbreaks have encouraged broader adoption of rapid diagnostic testing technologies. The presence of established diagnostic manufacturers and the continued expansion of testing capabilities across healthcare networks are also supporting market development.
Key companies participating in the Global Rapid Influenza Diagnostic Tests (RIDT) Market include Abbott, Siemens Healthineers, Roche, Quidel Corporation, Thermo Fisher Scientific, bioMerieux, Becton, Dickinson and Company (BD), DiaSorin, Meridian, Access Bio, CHEMBIO, 3B BlackBio, and SEKISUI. Companies operating in the Rapid Influenza Diagnostic Tests (RIDT) Market are adopting a range of strategies to strengthen their competitive position and expand their market presence. A major focus remains on research and development activities aimed at improving test sensitivity, accuracy, and speed. Many manufacturers are investing in advanced diagnostic technologies such as digital testing platforms and multiplex detection systems to enhance clinical value. Strategic collaborations with healthcare providers and diagnostic laboratories are helping companies broaden product adoption and improve distribution networks. In addition, organizations are expanding manufacturing capacity and strengthening supply chains to meet increasing global demand for rapid testing solutions. Companies are also emphasizing regulatory approvals and quality certifications to support product credibility and market entry.
Table of Contents
Chapter 1 Research Methodology
- 1.1 Research approach
- 1.2 Quality commitments
- 1.2.1 GMI AI policy & data integrity commitment
- 1.2.1.1 Source consistency protocol
- 1.2.1 GMI AI policy & data integrity commitment
- 1.3 Research trail & confidence scoring
- 1.3.1 Research trail components
- 1.3.2 Scoring components
- 1.4 Data collection
- 1.4.1 Partial list of primary sources
- 1.5 Data mining sources
- 1.5.1 Paid sources
- 1.5.1.1 Sources, by region
- 1.5.1 Paid sources
- 1.6 Base estimates and calculations
- 1.6.1 Base year calculation
- 1.7 Forecast model
- 1.7.1 Quantified market impact analysis
- 1.7.1.1 Mathematical impact of growth parameters on forecast
- 1.7.1 Quantified market impact analysis
- 1.8 Research transparency addendum
- 1.8.1 Source attribution framework
- 1.8.2 Quality assurance metrics
- 1.8.3 Our commitment to trust
Chapter 2 Executive Summary
- 2.1 Industry 360° synopsis
- 2.2 Key market trends
- 2.2.1 Regional trends
- 2.2.2 Product type trends
- 2.2.3 Technology trends
- 2.2.4 Sample type trends
- 2.2.5 End use trends
- 2.3 CXO perspectives: Strategic imperatives
Chapter 3 Industry Insights
- 3.1 Industry ecosystem analysis
- 3.2 Industry impact forces
- 3.2.1 Growth drivers
- 3.2.1.1 Growing prevalence of influenza
- 3.2.1.2 Technological advancements
- 3.2.1.3 Rising demand for early influenza diagnosis and management
- 3.2.1.4 Increasing popularity of rapid diagnostic tests
- 3.2.2 Industry pitfalls and challenges
- 3.2.2.1 Lack of skilled professionals
- 3.2.2.2 Stringent regulatory approvals
- 3.2.3 Opportunities
- 3.2.3.1 AI-enhanced interpretation tools for better accuracy
- 3.2.1 Growth drivers
- 3.3 Growth potential analysis
- 3.4 Regulatory landscape (Driven by primary research)
- 3.4.1 North America
- 3.4.2 Europe
- 3.4.3 Asia Pacific
- 3.5 Technology and innovation landscape
- 3.5.1 Current technological trends
- 3.5.2 Emerging technologies (Driven by primary research)
- 3.6 Future market trends (Driven by primary research)
- 3.7 Consumer behavior analysis
- 3.8 Value chain analysis
- 3.9 Pricing analysis, by products, 2025 (Driven by primary research)
- 3.10 Impact of AI & generative AI on the market (Driven by primary research)
- 3.10.1 AI-driven disruption of existing business models
- 3.10.2 GenAI use cases & adoption roadmap by segment
- 3.10.3 Risks, limitations & regulatory considerations
- 3.11 Gap analysis
- 3.12 Porter's analysis
- 3.13 PESTEL analysis
Chapter 4 Competitive Landscape, 2025
- 4.1 Introduction
- 4.2 Company matrix analysis
- 4.3 Company market share analysis
- 4.3.1 Global
- 4.3.2 North America
- 4.3.3 Europe
- 4.3.4 Asia Pacific
- 4.4 Competitive analysis of major market players
- 4.5 Competitive positioning matrix
- 4.6 Key developments
- 4.6.1 Mergers & acquisitions
- 4.6.2 Partnerships & collaborations
- 4.6.3 New product launches
- 4.6.4 Expansion plans
Chapter 5 Market Estimates and Forecast, By Product Type, 2022 - 2035 ($ Mn)
- 5.1 Key trends
- 5.2 Conventional RIDTs
- 5.3 Digital RIDTs
Chapter 6 Market Estimates and Forecast, By Technology, 2022 - 2035 ($ Mn)
- 6.1 Key trends
- 6.2 Immunochromatographic assays
- 6.3 Lateral flow assays
- 6.4 Polymerase Chain Reaction
- 6.5 Other technologies
Chapter 7 Market Estimates and Forecast, By Sample Type, 2022 - 2035 ($ Mn)
- 7.1 Key trends
- 7.2 Nasal Swab
- 7.3 Throat Swab
- 7.4 Other samples
Chapter 8 Market Estimates and Forecast, By End Use, 2022 - 2035 ($ Mn)
- 8.1 Key trends
- 8.2 Diagnostics centers
- 8.3 Hospitals
- 8.4 Research laboratories
- 8.5 Other end users
Chapter 9 Market Estimates and Forecast, By Region, 2022 - 2035 ($ Mn)
- 9.1 Key trends
- 9.2 North America
- 9.2.1 U.S.
- 9.2.2 Canada
- 9.3 Europe
- 9.3.1 Germany
- 9.3.2 UK
- 9.3.3 France
- 9.3.4 Spain
- 9.3.5 Italy
- 9.3.6 Netherlands
- 9.4 Asia Pacific
- 9.4.1 China
- 9.4.2 Japan
- 9.4.3 India
- 9.4.4 Australia
- 9.4.5 South Korea
- 9.5 Latin America
- 9.5.1 Brazil
- 9.5.2 Mexico
- 9.5.3 Argentina
- 9.6 MEA
- 9.6.1 South Africa
- 9.6.2 Saudi Arabia
- 9.6.3 UAE
Chapter 10 Company Profiles
- 10.1 3B BlackBio
- 10.2 Abbott
- 10.3 Access Bio
- 10.4 Becton, Dickinson and Company (BD)
- 10.5 bioMerieux
- 10.6 CHEMBIO
- 10.7 DiaSorin
- 10.8 Meridian
- 10.9 Quidel Corporation
- 10.10 Roche
- 10.11 SEKISUI
- 10.12 Siemens Healthineers
- 10.13 Thermo Fisher Scientific

