
|
시장보고서
상품코드
1836619
이탈리아의 체외진단 : 시장 점유율 분석, 산업 동향, 통계, 성장 예측(2025-2030년)Italy In-Vitro Diagnostics - Market Share Analysis, Industry Trends & Statistics, Growth Forecasts (2025 - 2030) |
||||||
 Mordor Intelligence
Mordor Intelligence
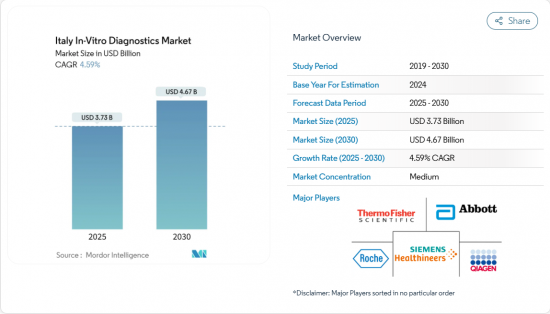
이탈리아의 체외진단 시장은 2025년에 37억 3,000만 달러로 평가되고, 2030년에는 46억 7,000만 달러에 이르며, CAGR 4.59%를 나타낼 것으로 예측됩니다.

성장을 지원하는 것은 만성 질환의 유병률 증가, 예방 검진의 꾸준한 증가, 납기를 단축하고 검사 메뉴를 넓히는 첨단 분자 플랫폼의 급속한 보급입니다. EU IVDR과의 규제 매칭은 단기 인증 비용을 증가시키지만 예측 기간 동안 제품 품질과 환자 안전을 향상시킬 것으로 기대됩니다. 기술의 융합, 특히 마이크로플루이딕스공학과 인공지능의 조합은 진단 정밀도를 높이면서 필요한 시료량을 계속 줄이고 있으며, 이 동향은 암 영역에 특화된 리퀴드 바이옵시나 멀티플렉스 PCR 검정에서 현저합니다. 한편, POC(point-of-care) 솔루션 수요는 지역 당국이 병원 네트워크의 용량 제약을 완화하기 위해 1차 케어나 가정에서의 진단에 접근하도록 추진하고 있기 때문에 가속화되고 있습니다.
이탈리아의 체외진단 시장 동향과 인사이트
만성·생활습관병(당뇨병, CVD, 암)의 부담 증가
만성질환은 현재 이탈리아 인구에서 차지하는 비율이 증가하고 있으며, 2024년에는 390만명이 당뇨병을 앓았고 심혈관질환은 여전히 사망 원인의 톱이 되고 있습니다. 증례 수가 증가함에 따라 지속적인 포도당 측정, 고감도 심장 마커 분석, 여러 위험 요인을 한 번에 프로파일링하는 다중 매개변수 패널 수요에 박차를 가하고 있습니다. 지불자는 연간 200억 유로 이상의 치료비를 억제하는 수단으로 진단을 캡처하고 있으며 조기 발견 도구에 대한 유리한 상환이 촉진되고 있습니다. 실험실에서는 대사 마커와 염증 마커를 동시에 분석하는 통합 플랫폼의 도입이 진행되고 있어 시약을 절약하면서 환자의 층별화를 개선하고 있습니다. 이와 같은 장기적인 역학적 변화는 일상 검사량의 꾸준한 증가를 지원하고 이탈리아의 체외진단용 의약품 시장 전체의 시약 수요를 안정시키고 있습니다.
분자 및 면역 진단의 급속한 기술 혁신
차세대 시퀀서와 멀티플렉스 PCR은 3차 시설에서 루틴 사용에 적합한 비용과 처리량 임계값에 도달하여 결과 시간을 단축하고 보다 광범위한 유전자 패널을 가능하게 했습니다. 마이크로플루이딕스 카트리지는 소아과 및 종양 생검에서 중요한 이점인 더 적은 양의 샘플을 처리할 수 있습니다. 이탈리아의 실험실은 종양학, 패혈증, 항균제 내성 패널을 위한 COVID 시대의 PCR 장치를 개장하여 시스템의 가동률이 향상되어 검사당 비용이 저하되었습니다. ImmunoDiagnostics는 시간당 최대 240건의 검사를 자동화하는 화학발광 플랫폼의 혜택을 받으며 불임, 갑상선 및 자가면역 마커에 대한 메뉴를 확대하고 있습니다. 유전체과 단백질체학 데이터가 통합됨에 따라, 임상의는 개인화된 의료 프로토콜에 반영된 풍부한 지식을 얻을 수 있으며, 분자 분석은 시장을 능가하는 성장을 유지하고 있습니다.
엄격히 진화하는 EU IVDR 규제 상황
IVDR은 대부분의 분석을 보다 엄격한 임상 증거 자료와 지속적인 시판 후 조사를 요구하는 고위험 클래스로 다시 분류하는 것입니다. 2024년까지 IVDR 인증을 받은 노티파이드 바디는 단 12개 기관으로 제품 상시를 지연시키는 신청 잔여물을 만들어 냈습니다. 중소기업에서는 컴플라이언스 비용이 연간 매출의 5-15%를 차지할 수 있으며, 새로운 시험에 자금을 제공하는 것보다 틈새 시험을 철회하도록 촉구될 수 있습니다. 다국적 대기업은 문서 업그레이드에 어려움을 겪고 있는 국내 동업자를 인수함으로써 점유율을 통합하기 위해 이 창구를 이용하고 있습니다. 마이그레이션 기한은 2029년까지 위험이 낮은 분석에서 늘어나지만, 시장 진입의 불확실성이 목표 투자 결정에 무거워질 수 있습니다.
부문 분석
면역 진단은 2024년 매출의 28%를 차지하며, 갑상선 질환, 불임, 감염 혈청 검사의 일상 패널을 지원했습니다. 안정적인 상환환경과 화학발광분석장치의 광범위한 설치기반은 한자리수 중반의 성장률로 부문의 성장을 지원하고 있습니다. 차세대 시퀀싱이 레퍼런스 랩에서 3차 병원으로 이동하고 종양학의 최소 잔존 병변 모니터링까지 커버 범위가 확대됨에 따라 분자진단학은 소규모 기반에서 시작되었지만 CAGR 7.8%로 성장을 지속하고 있습니다. 이탈리아의 체외진단용 의약품 시장은 증후성 호흡기 패널과 리퀴드 바이옵시의 보급을 반영하여 2025년부터 2030년까지 분자 분석에 기인하는 시장 규모가 두배로 될 것으로 예측됩니다. 컨버전스 동향에서 핵산 검출과 면역 포착 기술을 결합한 멀티플렉스 플랫폼을 통해 검사 시설은 장비 그룹을 통합하면서 메뉴의 폭을 넓힐 수 있습니다.
COVID-19 인프라(높은 처리량 PCR 사이클러 및 자동 추출기)는 성 감염 및 항균제 내성 검사에 재사용되어 활용도를 높입니다. 이탈리아 신흥기업은 시약량을 줄이는 마이크로플루이딕스칩 제조에 혁신을 가져와 예산에 중점을 둔 지역 의료 시스템에 호소하고 있습니다. 면역진단 벤더는 신경변성이나 신흥의 인수 공통 감염증을 타겟으로 한 고감도 분석으로 대응하고, 분자 벤더는 분석과 바이오인포매틱스를 번들한 제품으로 암 센터를 유치하고 있습니다. 이러한 역학은 이탈리아의 체외진단 시장에서 기술의 다원성을 강화하고 부문을 넘어서는 협력을 촉진합니다.
시약 및 소모품은 2024년 매출의 65%를 차지하며 공급업체의 현금 흐름을 안정시키는 정기적인 수요 패턴이 이 점유율을 견인했습니다. 만성 질환 모니터링에서 검사량이 증가하면 로트 크기가 증가하고 실험실이 대량 구매 할인을 협상하는 데 도움이 됩니다. 그러나 많은 분석기는 폐쇄 시스템이기 때문에 공급업체의 가격 결정력이 유지되고 60%를 초과하는 조율이 유지되고 있습니다. 장비 및 분석 장비의 CAGR은 6.5%이지만, 이는 시설이 시간당 3,000개의 자동 추적 시스템으로 현대화되어 인력 부족을 완화하고, 시료당 비용을 낮추고 있기 때문입니다. 소프트웨어와 인포매틱스 솔루션(미들웨어부터 AI 대응 의사결정 지원까지)은 가장 이익률이 높은 카테고리로 등장하며 자본 지출을 영업예산으로 옮기는 재렌탈 계약에 번들 되는 경우가 많습니다.
대학병원에서는 수작업으로 인한 실수를 20% 줄이는 전자동 검사 라인이 인기를 끌고 있습니다. 클라우드에서 제공되는 품질 관리 대시보드는 지역 보건 당국이 실험실 성능을 모니터링하는 데 도움이 됩니다. 오픈 플랫폼 제창자들은 비용 절감을 위해 시약의 상호 운용성을 추진하고 있지만, 공급업체는 수명 주기 수익원을 선호하기 때문에 독자적인 시약 전략이 여전히 보급되고 있습니다.
기타 혜택 :
- 엑셀 형식 시장 예측(ME) 시트
- 3개월의 애널리스트 지원
목차
제1장 서론
- 조사 전제조건과 시장 정의
- 조사 범위
제2장 조사 방법
제3장 주요 요약
제4장 시장 상황
- 시장 개요
- 시장 성장 촉진요인
- 만성질환·생활습관병(당뇨병, CVD, 암)의 부담증
- 분자·면역 진단에 있어서의 급속한 기술 혁신
- 1차 의료 및 재택 의료 환경에서의 POC(Point-of-Care) 검사의 확대
- 디지털 실험실 현대화를 위한 정부와 EU 투자 프로그램
- 정밀의료와 동반진단의 채용 확대
- 시장 성장 억제요인
- EU의 IVDR 규제 상황의 엄격함과 진화
- 지역적 상환 지연과 예산 제약
- 숙련된 임상검사기사의 부족과 트레이닝 갭
- 규제 전망
- Porter's Five Forces 분석
- 신규 참가업체의 위협
- 구매자의 협상력
- 공급기업의 협상력
- 대체품의 위협
- 경쟁 기업 간 경쟁 관계
제5장 시장 규모·성장 예측(금액, 달러)
- 검사 유형별
- 임상 화학
- 면역진단
- 분자진단
- 혈액학
- 미생물학
- 응고
- POC(Point-of-Care) 검사
- 제품별
- 기기 및 분석기
- 시약 및 소모품
- 소프트웨어 및 서비스
- 사용성별
- 일회용 체외진단 기기
- 재사용 가능 체외진단 기기
- 검사 방식별
- 실험실 기반 검사
- POC(Point-of-Care) 검사
- 용도별
- 감염성 질환
- 당뇨병
- 종양학(암)
- 심장학
- 자가면역 질환
- 기타 용도
- 최종 사용자별
- 병원 및 클리닉
- 진단 실험실
- 학술 및 연구 기관
- 재택 케어/외래 POC 환경
- 기타 최종 사용자
제6장 경쟁 구도
- 시장 집중도
- 시장 점유율 분석
- 기업 프로파일
- F. Hoffmann-La Roche AG
- Abbott Laboratories
- Siemens Healthineers AG
- Danaher Corp.(Beckman Coulter & Cepheid)
- DiaSorin SpA
- BioMerieux SA
- Thermo Fisher Scientific Inc.
- Sysmex Corporation
- QIAGEN NV
- Becton, Dickinson and Company
- Werfen SA
- Menarini Diagnostics Srl
- Sentinel Diagnostics SpA
- Alfa Wassermann Diagnostic Technologies
- Sentinel CH SpA
- Luminex(DiaSorin Group)
- Randox Laboratories Ltd
- Bio-Rad Laboratories Inc.
- Illumina Inc.
- Agilent Technologies Inc.
- DIESSE Diagnostica Senese SpA
- Sclavo Diagnostics International
제7장 시장 기회와 전망
KTH 25.11.04The Italy in vitro diagnostics market is valued at USD 3.73 billion in 2025 and is forecast to reach USD 4.67 billion by 2030, expanding at a 4.59% CAGR.
Growth is sustained by the rising prevalence of chronic diseases, steady gains in preventive health screening, and rapid uptake of advanced molecular platforms that cut turnaround times and broaden test menus. Regulatory alignment with the EU IVDR is adding short-term certification costs yet is expected to improve product quality and patient safety over the forecast horizon. Technology convergence, particularly the pairing of microfluidics with artificial intelligence, continues to lower sample-volume requirements while boosting diagnostic accuracy, a trend most visible in oncology-focused liquid biopsy and multiplex PCR assays. Meanwhile, demand for point-of-care (POC) solutions is accelerating as regional authorities push diagnostics closer to primary-care and home settings to relieve capacity constraints in the hospital network.
Italy In-Vitro Diagnostics Market Trends and Insights
Rising Burden of Chronic & Lifestyle Diseases (Diabetes, CVD, Cancer)
Chronic conditions now affect a growing share of Italy's population, with 3.9 million residents living with diabetes in 2024 and cardiovascular disease remaining the top cause of mortality. Larger case volumes have spurred demand for continuous glucose-monitoring, high-sensitivity cardiac-marker assays, and multi-parameter panels that profile several risk factors in one run. Payers see diagnostics as a lever to curb treatment costs exceeding EUR 20 billion per year, fostering favorable reimbursement for early-detection tools. Laboratories increasingly deploy integrated platforms that simultaneously analyze metabolic and inflammatory markers, improving patient stratification while conserving reagents. This long-term epidemiological shift underpins steady increases in routine test volumes, thereby stabilizing reagent demand across the Italy in vitro diagnostics market.
Rapid Technological Innovation in Molecular & Immunodiagnostics
Next-generation sequencing and multiplex PCR have reached cost and throughput thresholds suited for routine use in tertiary centers, cutting time-to-result and enabling wider gene panels. Microfluidic cartridges now process smaller sample volumes, a crucial advantage in pediatrics and oncology biopsies. Italian labs are retrofitting COVID-era PCR instruments for oncology, sepsis, and antimicrobial-resistance panels, which lifts system utilization and lowers per-test costs. Immunodiagnostics benefit from chemiluminescent platforms that automate up to 240 tests per hour, expanding menus into fertility, thyroid, and autoimmune markers. As genomic and proteomic data converge, clinicians gain richer insights that feed into personalized-medicine protocols, sustaining above-market growth for molecular assays.
Stringent & Evolving EU IVDR Regulatory Landscape
The IVDR recasts most assays into higher-risk classes that demand stricter clinical-evidence dossiers and ongoing post-market surveillance. Only 12 notified bodies were approved for IVDR certification by 2024, creating application backlogs that slow product launches. Compliance expenses can absorb 5-15% of annual revenue for smaller firms, prompting some to withdraw niche tests rather than fund new studies. Larger multinationals use this window to consolidate share by acquiring domestic peers struggling with documentation upgrades. Although transition deadlines stretch to 2029 for low-risk assays, market-access uncertainty weighs on near-term investment decisions.
Other drivers and restraints analyzed in the detailed report include:
- Expansion of Point-of-Care Testing Across Primary & Home Settings
- Government & EU Investment Programs for Digital Lab Modernization
- Regional Reimbursement Delays & Budget Constraints
For complete list of drivers and restraints, kindly check the Table Of Contents.
Segment Analysis
Immunodiagnostics commanded 28% of 2024 revenue, underpinning routine panels for thyroid disorders, fertility, and infectious-disease serology. The stable reimbursement environment and broad installed base of chemiluminescent analyzers anchor segment growth at mid-single-digit rates. Molecular diagnostics, though starting from a smaller base, is charting a 7.8% CAGR as next-generation sequencing migrates from reference labs to tertiary hospitals, extending coverage into oncology minimal-residual-disease monitoring. The Italy in vitro diagnostics market size attributed to molecular assays is expected to double between 2025 and 2030, reflecting expanded syndromic respiratory panels and liquid biopsy uptake. Convergence trends see multiplex platforms combining nucleic-acid detection with immuno-capture technologies, enabling laboratories to consolidate instrument fleets while widening their menus.
COVID-19 infrastructure-high-throughput PCR cyclers and automated extractors-is now repurposed for sexually transmitted infections and antimicrobial-resistance testing, lifting utilization rates. Italian start-ups innovate in microfluidic chip fabrication that slashes reagent volumes, appealing to budget-conscious regional health systems. Immunodiagnostic suppliers respond with high-sensitivity assays targeting neurodegeneration and emerging zoonoses, while molecular vendors court oncology centers with bundled assay-plus-bioinformatics offerings. Such dynamics reinforce technology pluralism and foster cross-segment collaboration within the Italy in vitro diagnostics market.
Reagents and consumables generated 65% of turnover in 2024, a share driven by recurring demand patterns that stabilize cash flows for suppliers. Rising test volumes in chronic-disease monitoring lift lot sizes, helping laboratories negotiate bulk-purchase discounts. Still, the closed-system philosophy of many analyzers preserves vendor pricing power and sustains gross margins that often exceed 60%. Instruments and analyzers post a 6.5% CAGR as facilities modernize to automated track systems capable of 3,000 tubes per hour, mitigating staff shortages and lowering per-sample cost. Software and informatics solutions-ranging from middleware to AI-enabled decision support-emerge as the highest-margin category and are frequently bundled under reagent-rental contracts that shift capital expenditure into operating budgets.
Total-laboratory-automation lines gain favor in university hospitals, where they drive 20% reductions in manual handling errors. Cloud-delivered quality-control dashboards help regional health authorities monitor laboratory performance, a feature aligning well with new IVDR post-market surveillance rules. Open-platform advocates push for reagent interoperability to reduce costs, yet proprietary-reagent strategies remain prevalent as suppliers prioritize life-cycle revenue streams.
The Italy In-Vitro Diagnostics Market Report is Segmented by Test Type (Clinical Chemistry, Molecular Diagnostics, and More), Product (Instruments & Analyzers, and More), Usability (Disposable IVD Devices and Reusable IVD Devices), Application (Infectious Disease, Diabetes, and More. ), Mode of Testing (Laboratory-Based Testing and Point-Of-Care Testing), and End-Users (Diagnostic Laboratories, Hospitals and Clinics, and More).
List of Companies Covered in this Report:
- Roche
- Abbott Laboratories
- Siemens Healthineers
- Danaher Corp. (Beckman Coulter & Cepheid)
- DiaSorin
- bioMerieux
- Thermo Fisher Scientific
- Sysmex
- QIAGEN
- Beckton Dickinson
- Werfen S.A.
- Menarini Diagnostics S.r.l.
- Sentinel Diagnostics S.p.A.
- Alfa Wassermann Diagnostic Technologies
- Sentinel CH S.p.A.
- Luminex (DiaSorin Group)
- Randox Laboratories
- Bio-Rad Laboratories
- Illumina
- Agilent Technologies
- DIESSE Diagnostica Senese S.p.A.
- Sclavo Diagnostics International
Additional Benefits:
- The market estimate (ME) sheet in Excel format
- 3 months of analyst support
TABLE OF CONTENTS
1 Introduction
- 1.1 Study Assumptions & Market Definition
- 1.2 Scope of the Study
2 Research Methodology
3 Executive Summary
4 Market Landscape
- 4.1 Market Overview
- 4.2 Market Drivers
- 4.2.1 Rising Burden of Chronic & Lifestyle Diseases (Diabetes, CVD, Cancer)
- 4.2.2 Rapid Technological Innovation in Molecular & Immunodiagnostics
- 4.2.3 Expansion of Point-of-Care Testing Across Primary & Home Settings
- 4.2.4 Government & EU Investment Programs for Digital Lab Modernization
- 4.2.5 Growth of Precision Medicine & Companion Diagnostics Adoption
- 4.3 Market Restraints
- 4.3.1 Stringent & Evolving EU IVDR Regulatory Landscape
- 4.3.2 Regional Reimbursement Delays & Budget Constraints
- 4.3.3 Shortage of Skilled Laboratory Personnel & Training Gaps
- 4.4 Regulatory Outlook
- 4.5 Porter's Five Forces Analysis
- 4.5.1 Threat of New Entrants
- 4.5.2 Bargaining Power of Buyers
- 4.5.3 Bargaining Power of Suppliers
- 4.5.4 Threat of Substitutes
- 4.5.5 Competitive Rivalry Intensity
5 Market Size & Growth Forecasts (Value, USD)
- 5.1 By Test Type
- 5.1.1 Clinical Chemistry
- 5.1.2 Immunodiagnostics
- 5.1.3 Molecular Diagnostics
- 5.1.4 Hematology
- 5.1.5 Microbiology
- 5.1.6 Coagulation
- 5.1.7 Point-of-Care (POC) Tests
- 5.2 By Product
- 5.2.1 Instruments & Analyzers
- 5.2.2 Reagents & Consumables
- 5.2.3 Software & Services
- 5.3 By Usability
- 5.3.1 Disposable IVD Devices
- 5.3.2 Reusable IVD Devices
- 5.4 By Mode of Testing
- 5.4.1 Laboratory-Based Testing
- 5.4.2 Point-of-Care Testing
- 5.5 By Application
- 5.5.1 Infectious Disease
- 5.5.2 Diabetes
- 5.5.3 Oncology (Cancer)
- 5.5.4 Cardiology
- 5.5.5 Autoimmune Disorders
- 5.5.6 Other Applications
- 5.6 By End-User
- 5.6.1 Hospitals & Clinics
- 5.6.2 Diagnostic Laboratories
- 5.6.3 Academic & Research Institutes
- 5.6.4 Home-Care / Ambulatory POC Settings
- 5.6.5 Other End-Users
6 Competitive Landscape
- 6.1 Market Concentration
- 6.2 Market Share Analysis
- 6.3 Company Profiles (includes Global-level Overview, Market-level Overview, Core Segments, Financials as available, Strategic Information, Market Rank/Share, Products & Services, Recent Developments)
- 6.3.1 F. Hoffmann-La Roche AG
- 6.3.2 Abbott Laboratories
- 6.3.3 Siemens Healthineers AG
- 6.3.4 Danaher Corp. (Beckman Coulter & Cepheid)
- 6.3.5 DiaSorin S.p.A
- 6.3.6 BioMerieux SA
- 6.3.7 Thermo Fisher Scientific Inc.
- 6.3.8 Sysmex Corporation
- 6.3.9 QIAGEN N.V.
- 6.3.10 Becton, Dickinson and Company
- 6.3.11 Werfen S.A.
- 6.3.12 Menarini Diagnostics S.r.l.
- 6.3.13 Sentinel Diagnostics S.p.A.
- 6.3.14 Alfa Wassermann Diagnostic Technologies
- 6.3.15 Sentinel CH S.p.A.
- 6.3.16 Luminex (DiaSorin Group)
- 6.3.17 Randox Laboratories Ltd
- 6.3.18 Bio-Rad Laboratories Inc.
- 6.3.19 Illumina Inc.
- 6.3.20 Agilent Technologies Inc.
- 6.3.21 DIESSE Diagnostica Senese S.p.A.
- 6.3.22 Sclavo Diagnostics International
7 Market Opportunities & Future Outlook
- 7.1 White-Space & Unmet-Need Assessment
