
|
시장보고서
상품코드
1830067
이중 특이성 항체 시장 : 업계 동향과 세계 예측(-2035년) - 치료 영역별, 작용기전별, 표적 항원 항체 형태별, 주요 지역별, 주요 기업별Bispecific Antibodies Market: Industry Trends and Global Forecasts, Till 2035 - Distribution by Therapeutic Area, Mechanism of Action, Target Antigen Antibody Format, Key Geographical Regions and Key Players |
||||||
이중 특이성 항체 시장 개요
세계 이중 특이성 항체 시장 규모는 2035년까지 예측 기간 동안 6.5%의 연평균 복합 성장률(CAGR)로 확대되어 현재 89억 3,000만 달러에서 2035년까지 168억 1,000만 달러로 성장할 것으로 예측됩니다.
시장 세분화에서는 시장 규모 및 기회 분석을 다음과 같은 매개 변수로 구분합니다.
치료 영역
- 자가면역 질환
- 유전성 질환
- 혈액 악성 종양
- 안과 질환
- 피부암
- 고형 종양
작용기전
- 사이토카인 재표적화/중화
- 이중 리간드 차단
- 내성 인자 공동 표적화
- 종양 혈관신생 표적화
- T세포 재표적화/활성화
- 기타
표적 항원
- C5-Albumin
- CD20 x CD3
- CD3 x BCMA
- CD3 x CD19
- EGFR x cMET
- EpCAM x CD3
- Factor IXa x Factor X
- gp100 x CD3
- HER2 x HER2
- PD-1 x CTLA-4
- PD-L1 x TGFB
- TNF-a x HSA
- VEGF x DLL4
- VEGF-A x ANG2
항체 형태
- 비대칭
- 조각
지역
- 북미(미국, 캐나다, 기타)
- 유럽(독일, 프랑스, 이탈리아, 스페인, 영국, 기타)
- 아시아(인도, 중국, 일본, 한국, 기타)
- 기타 지역
이중 특이성 항체 시장 성장 및 동향
단일 클론 항체의 치료 능력을 평가하고 많은 질병의 치료에 효과적으로 적용함으로써 제약 분야는 변모하고 있습니다. 현재 치료 효과를 높이기 위한 인공 항체 치료제 개발을 위해 광범위한 조사가 진행되고 있습니다. 수십년전, 단일클론항체에 항원 결합 부위를 추가하여 2가 항체가 개발되었습니다. 이 2가 분자의 주요 목적은 세포 독성 면역 이펙터 세포를 유도하고, 항체 의존성 세포 매개 세포 손상(ADCC) 및 면역 이펙터 세포에 의해 구동되는 다양한 다른 세포 손상 과정을 통해 종양 세포의 파괴를 강화하는 것이었습니다. 이 항체 기반 치료법의 개선된 버전은 현재 제약회사로부터 큰 관심을 받고 있습니다. 최근 다양한 표적 질환에 대한 혁신적인 이중 특이성 항체 치료제가 임상시험에서 큰 이점을 가져다주는 것으로 나타나면서, 이러한 치료법 개발에 종사하는 사람들에게 큰 기회를 제공합니다.
이특이성 항체 시장은 혈액암, 자가면역질환, 기타 질환에 대한 맞춤의료에 대한 관심 증가, 암 부담 증가 등의 주요 요인에 의해 주도되고 있습니다. 만성질환의 경제적 부담과 사망률에 미치는 영향이 증가함에 따라 다양한 종양학 및 비종양학 질환에 대응할 수 있는 효율적인 이특이적 항체 치료제의 필요성이 증가하고 있습니다. 그 결과, 효율적인 이특이성 항체 치료에 대한 수요 증가와 함께 산업계와 비산업계 모두의 연구개발 이니셔티브가 향후 10년간 이특이성 항체 시장을 주도할 것으로 예측됩니다.
이특이성 항체 시장 주요 인사이트
본 보고서에서는 이중 특이성 항체 시장의 현황을 조사하고, 이중 특이성 항체 시장의 잠재적 성장 기회를 파악하고자 합니다. 본 보고서의 주요 조사 결과는 다음과 같습니다.
- 이중 특이성 항체 치료제의 상황은 지난 10년간 꾸준히 발전해 왔으며, 전 세계 120개 이상의 제약회사에서 400개 이상의 임상/전임상 후보물질이 평가되고 있습니다.
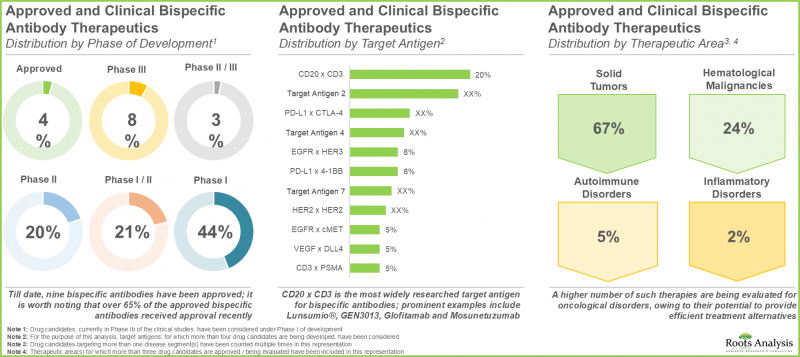
- 현재 파이프라인에는 다양한 생물학적 항원을 표적으로 하여 여러 적응증을 치료할 수 있는 임상 단계의 이중 특이성 항체 의약품 후보물질이 다수 존재합니다.
- 실제로 업계 관계자들은 85개 이상의 이특이성 항체 기술 플랫폼 개발에 참여하고 있으며, 이러한 치료와 관련된 기존 제조상의 문제를 완화하는 것을 목표로 하고 있습니다.
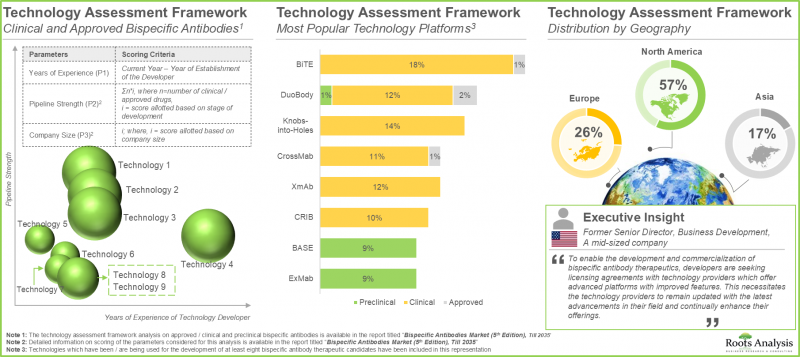
- 관심이 높아진 것은 제휴 활동이 활발해지면서 이중 특이성 항체 포트폴리오를 확대하기 위해 기업들이 적극적으로 전략적 계약을 체결하고 있는 것에서도 알 수 있습니다.
- 2010년 이후 다양한 이중 특이성 항체 치료제의 안전성과 유효성을 평가하기 위해 약 280건의 임상시험이 등록되었으며, 대부분 미국 내에서 진행되었습니다.
- 이러한 치료법을 효율적으로 보급하기 위해 의약품 개발 기업들은 시장에서의 지위를 유지하기 위해 다양한 홍보 전략을 적극적으로 모색하고 있습니다.
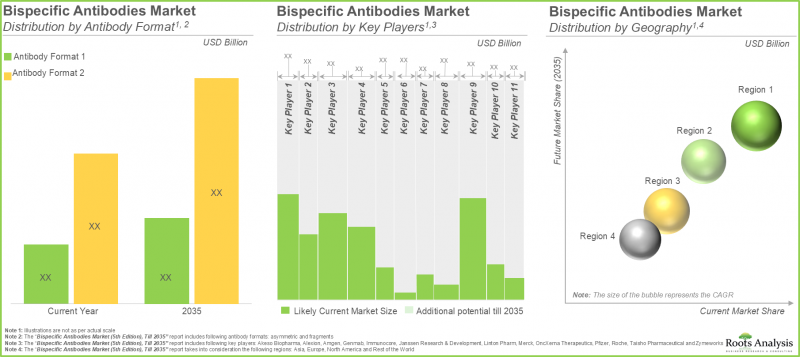
- 개발 파이프라인에 대한 관심 증가와 유망한 임상 결과들로 인해 향후 10년간 연평균 6.5% 이상 성장할 것으로 예측됩니다.
이중 특이성 항체 시장 주요 부문
혈액악성종양은 이중 특이성 항체 시장에서 가장 빠르게 성장하는 분야입니다.
치료 분야별로 시장은 자가면역질환, 유전질환, 혈액악성종양, 안과질환, 피부암, 고형암으로 구분됩니다. 현재 이중 특이성 항체 시장에서 유전자 질환이 가장 큰 비중을 차지하고 있습니다. 혈액악성종양 이특이성 항체 시장은 비교적 높은 CAGR로 성장할 가능성이 높다는 점은 주목할 만합니다.
예측 기간 동안 T 세포의 재표적화/활성화를 통해 작용하는 이중 특이성 항체가 가장 큰 비중을 차지할 것으로 예측됩니다.
작용기전 측면에서 시장은 사이토카인 재표적화/중화, 이중 리간드 차단, 내성 인자 공동 표적화, 종양 혈관신생 표적화, T세포 재표적화/활성화, 기타 활동으로 구분됩니다. 현재 이중 특이성 항체 시장에서 T세포 재표적화/활성화가 가장 큰 비중을 차지하고 있습니다. 그러나 가까운 미래에는 사이토카인의 재표적화/중화를 통해 작용하는 이중 특이성 항체가 가장 높은 시장을 점유할 것으로 예측됩니다.
CD3 x BCMA를 표적으로 하는 이중 특이성 항체가 시장에서 가장 빠르게 성장하는 분야로 떠오름
표적 항원 측면에서 시장은 C5-알부민, CD20 x CD3, CD3 x BCMA, CD3 x CD19, EGFR x cMET, EpCAM x CD3, 제IXa 인자 x X인자, gp100 x CD3, HER2 x HER2, PD-1 x CTLA-4, PD-L1 x TGFB, TNF-a x HSA, VEGF x DLL4, VEGF-A x ANG2로 구분됩니다. 현재 이중 특이성 항체 시장에서 가장 큰 비중을 차지하는 것은 제IXa인자×제X인자를 표적으로 하는 치료제입니다. CD3 x BCMA를 표적으로 하는 약물은 상대적으로 높은 CAGR로 성장할 가능성이 높다는 점은 주목할 만합니다.
예측 기간 동안 비대칭 이중 특이성 항체가 시장을 독점할 가능성이 높습니다.
항체 형식에 관해서는 시장은 비대칭형과 단편형으로 구분됩니다. 현재 이중 특이성 항체 시장에서 비대칭 항체가 가장 큰 점유율을 차지하고 있습니다. 이 추세는 당분간 변하지 않을 것 같습니다.
북미가 가장 큰 점유율을 차지
주요 지역별로 시장은 북미, 유럽, 아시아태평양 및 기타 지역으로 분류됩니다. 북미가 이중 특이성 항체 시장의 대부분을 차지할 것으로 예측됩니다. 또한, 유럽이 향후 몇 년 동안 더 높은 CAGR로 성장할 것으로 예상된다는 점은 주목할 만합니다.
이중 특이성 항체 시장 진출기업 사례
- Akeso Biopharma
- Alexion
- Amgen
- Genmab
- Immunocore
- Janssen Research & Development
- Linton Pharm
- Merck
- OncXerna Therapeutics
- Pfizer
- Roche
- Taisho Pharmaceutical
- Zymeworks
1차 조사 개요
본 조사에서 제시된 의견과 통찰력은 여러 이해관계자와의 논의를 통해 영향을 받았습니다. 본 조사 보고서에는 다음과 같은 업계 이해관계자들과의 상세한 인터뷰 기록이 수록되어 있습니다.
- A사 수석 과학자, A사
- 사업개발 컨설턴트, B사
- C사 이사(GMP 임상 제조), C사
- D사 전 사업개발 시니어 디렉터
- E사, 창업자 겸 최고과학책임자 겸 최고경영자(CEO)
- F사 박사과정 재학
이중 특이성 항체 시장 조사 대상
- 시장 규모 및 기회 분석 본 보고서는(A) 치료 영역,(B) 작용기전,(C) 표적 항원,(D) 항체 형태,(E) 주요 지역 등 주요 시장 부문에 초점을 맞추어 이중 특이성 항체 시장을 상세하게 분석합니다.
- 시장현황1: 승인되었거나 임상개발 단계에 있는 이중 특이성 항체를(A)개발사,(B)개발단계,(C)표적항원,(D)치료유형,(E)투여경로,(F)투여방법,(G)표적 적응증,(H)치료영역,(I)질환군,(J)설립연도,(K)기업규모,(L)본사 소재지 등 다양한 파라미터를 고려하여 종합적으로 평가.
- 시장 상황 2: 현재 전임상시험 중인 이중 특이성 항체를(A) 개발사,(B) 개발 단계,(C) 표적 항원,(D) 치료 영역,(E) 질환 분야,(F) 설립 연도,(G) 기업 규모,(H) 개발사 본사 소재지 등 다양한 파라미터를 고려하여 종합적으로 평가.
- 주요 인사이트 A) 개발 단계 및 투여 경로,(B) 개발 단계 및 질병 부문,(C) 개발 단계 및 본사 소재지 등 관련 파라미터를 기반으로 이중 특이성 항체 치료제 시장 동향을 상세하게 분석합니다. 또한, 본 장에서는(D) 개발 단계와 질환 부문,(E) 개발 단계와 본사 소재지에 따라 전임상 단계의 이중 특이성 항체 치료제를 다양하게 표현하고 있습니다. 또한, 본 장에서는(F) 개발 단계(전임상, 임상, 전임상/임상),(G) 본사 소재지를 기준으로 이중 특이성 항체 치료제 개발 기업에 대해서도 기술하였습니다.
- 기술평가 프레임워크: A) 임상/임상 전단계 파이프라인의 강점, B) 개발사의 경력기간, C) 기업규모, D) 개발사의 본사 소재지 등 여러 관련 파라미터를 기반으로 다양한 제약개발기업이 이중 특이성 항체치료제 제조를 위해 개발/사용하고 있는 기술플랫폼을 상세하게 평가 평가합니다.
- 빅파마 분석 : 주요 제약사별 이중 특이성 항체 치료제에 초점을 맞춘 다양한 이니셔티브를 종합적으로 검토. 이 분석에는 주요 제약사의 분포를 보여주는 히트맵 시각화, 여러 관련 매개변수에 대한 이니셔티브를 비교하는 스파이더웹 다이어그램 등이 포함됩니다.
- 기업 프로파일: A) 기업 개요, B) 재무 정보(가능한 경우), C) 의약품 포트폴리오, D) 최근 동향, E) 정보에 입각한 미래 전망에 초점을 맞춘 다양한 지역의 이특이성 항체 개발에 종사하는 주요 기업 프로파일을 상세하게 수록했습니다.
- 파트너십 및 협업A)파트너십 체결 연도,(B)파트너십 유형,(C)질병 부문,(D)채택된 지불 모델 유형,(E)거래 금액,(F)가장 활발한 기업(체결된 거래 수),(G)가장 인기 있는 기술(체결된 기술 관련) 거래 건수) 등 몇 가지 매개변수를 기반으로 2016년 이후 이 분야에서 구축된 파트너십을 분석하였습니다. 이 섹션에서는 이 시장에서의 파트너십 활동의 지역적 분포도 확인할 수 있습니다.
- 이중 특이성 항체 치료제 계약 서비스: 이중 특이성 항체 생산과 관련된 주요 단계 및 과제에 대한 검토. 또한, 이중 특이성 항체 개발자가 적절한 CRO/CMO를 선택할 때 고려해야 할 주요 사항을 강조하고, 제조수탁기관(CMO) 및 생물학적제제 연구개발수탁기관(CRO) 리스트를 수록하였습니다.
- 임상시험 분석 A) 임상시험 등록 연도, B) 임상시험 단계, C) 임상시험 모집 현황, D) 등록 환자 수, E) 임상시험 유형, F) 임상시험 설계, G) 스폰서/공동연구자 유형, H) 주요 산업 및 비산업계 참여 기업, I) 주요 중점 분야, J) 임상시험의 지리적 위치 등 매개변수를 기반으로 다양한 이특이성 항체 치료제에 대한 완료, 진행 중, 계획 중인 임상시험을 조사했습니다.
- 사례 연구 1: 이중 특이성 항체 개발과 관련하여 ICH, WHO, FDA가 발표한 일반적인 규제 가이드라인에 대한 고찰. 또한, FDA 가이드라인에 대한 다양한 제약업계의 대응에 대해서도 자세히 설명하고 있습니다.
- 사례 연구 2: 승인된 이중 특이성 항체인 Blincyto(R)와 Hemlibra(R)의 개발자들이 채택하고 있는 다양한 홍보 전략과 두 약품의 비교, 각 웹 사이트에서 제공되는 정보를 바탕으로 한 두 약품의 비교, 그리고 그러한 노력을 하고 있는 기업의 사례. 시판 중인 이중 특이성 항체의 홍보에 사용되는 다양한 채널을 검토하고 있습니다.
- SWOT 분석 : SWOT 분석은 산업 발전에 영향을 미칠 수 있는 주요 촉진요인과 과제에 초점을 맞추었습니다. 또한, 각 SWOT 매개변수가 산업 전체에 미치는 상대적인 영향을 강조하는 하비볼 분석도 게재되어 있습니다.
목차
제1장 서문
제2장 주요 요약
제3장 서론
- 본 장의 개요
- 항체 서론
- 항체 치료제
- 이중 특이성 항체 형태
- 이중 특이성 항체 치료제 작용기전
- 이중 특이성 항체 응용
제4장 승인이 끝난 상태 및 임상 치료 시장 구도
- 본 장의 개요
- 승인이 끝난 상태 및 임상 단계 이중 특이성 항체 치료제 : 시장 구도
- 승인이 끝난 상태 및 임상 단계 이중 특이성 항체 치료제 : 개발 기업 전체 상황
제5장 전임상 치료 시장 구도
- 본 장의 개요
- 전임상 이중 특이성 항체 치료제 : 시장 구도
- 전임상 이중 특이성 항체 치료제 : 개발 상황 전체 상황
제6장 주요 인사이트
- 본 장의 개요
- 승인 상태 및 임상 단계 이중 특이성 항체 치료제 상황 : 주요 인사이트
- 전임상 단계 이중 특이성 항체 치료제 상황 : 주요 인사이트
- 이중 특이성 항체 치료제 개발 상황 : 주요 인사이트
제7장 기술 평가 프레임워크
- 본 장의 개요
- 이중 특이성 항체 치료제 : 기술 플랫폼 리스트
- 이중 특이성 항체 기술 플랫폼 : 비교 분석
- 가장 인기 있는 기술 플랫폼 : 개발 단계별 분석
- 이중 특이성 항체 기술 플랫폼 개발 기업 : 본사 소재지별 분석
제8장 대형 제약 기업 : 벤치마킹 분석
- 본 장의 개요
- 대형 제약 기업 : 벤치마킹 분석(Spider Web Representation)
- 대형 제약 기업 : 임상 파이프라인 비교 분석
제9장 기업 개요
- 본 장의 개요
- Akeso Biopharma
- Alphamab Oncology
- Amgen
- Merck
- Regeneron
- Roche
- Xencor
제10장 파트너십 및 협업
- 본 장의 개요
- 파트너십 모델
- 이중 특이성 항체 치료제 : 파트너십 및 협업
제11장 이중 특이성 항체 치료제에 관한 계약 서비스
- 본 장의 개요
- 이중 특이성 항체 치료제 제조
- 적절한 CMO/CRO 파트너를 선택하기 위한 중요 고려사항
제12장 임상시험 분석
- 본 장의 개요
- 주요 전제와 조사 방법
- 이중 특이성 항체 치료제 : 임상시험 분석
제13장 사례 연구 : 이중 특이성 항체에 관한 규제 가이드라인
- 본 장의 개요
- 규제기관이 발행한 가이드라인
- 미국 식품의약국(FDA)
- 세계보건기구(WHO)
제14장 사례 연구 : 프로모션/마케팅 전략
- 본 장의 개요
- 프로모션 캠페인에 사용되는 주요 채널
- 프로모션 및 마케팅 전략에 사용되는 기타 채널
- 요약 : 이중 특이성 항체 개발자가 활용하는 프로모션 및 마케팅 전략
- 프로모션 분석 : Blincyto(R)
- 프로모션 분석 : Hemlibra(R)
제15장 시장 예측과 기회 분석
- 본 장의 개요
- 범위와 제한
- 예측 조사 방법과 주요 전제조건
- 이중 특이성 항체 치료제 시장, 2035년까지
- 이중 특이성 항체 시장 : 가치 창조 분석
- 이중 특이성 항체 치료제 시장 : 제품별 판매 예측
- AK104 (Akeso Biopharma)
- Blincyto(TM) (Amgen)
- Hemlibra(R) (Roche)
- Kimmtrak(R) (Immunocore)
- Lunsumio(R) (Roche)
- Nanozora(R) (Taisho Pharmaceutical)
- Rybrevant(TM) (Janssen Research & Development)
- Tecvayli(TM) (Janssen Research & Development)
- Vabysmo(TM) (Roche)
- AK112 (Akeso Biopharma)
- ALXN1720 (Alexion)
- GEN3013 (Genmab)
- Glofitamab (Roche)
- LP000 (Linton Pharm)
- M7824 (Merck)
- OMP 305B83 (Mereo BioPharma)
- PF-06863135 (Pfizer)
- ZW25 (Zymeworks)
- 결론
제16장 SWOT 분석
- 본 장의 개요
- 강점
- 약점
- 기회
- 위협
- 결론
제17장 결론
제18장 경영진 인사이트
제19장 부록 1 : 표 형식 데이터
제20장 부록 2 : 기업 및 조직 리스트
LSH 25.10.16Bispecific Antibodies Market: Overview
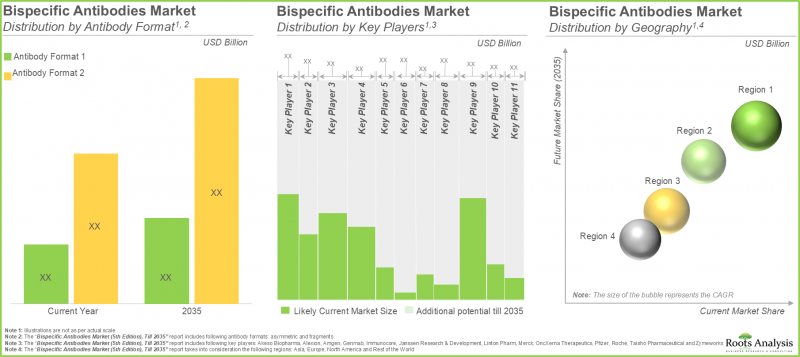
As per Roots Analysis, the global bispecific antibodies market is estimated to grow from USD 8.93 billion in the current year to USD 16.81 billion by 2035, at a CAGR of 6.5% during the forecast period, till 2035.
The market sizing and opportunity analysis has been segmented across the following parameters:
Therapeutic Area
- Autoimmune Disorders
- Genetic Disorders
- Hematological Malignancies
- Ophthalmic Disorders
- Skin Cancers
- Solid Tumors
Mechanism of Action
- Cytokines Retargeting / Neutralization
- Dual Ligands Blocking
- Resistance Factors Co-targeting
- Targeting Tumor Angiogenesis
- T-Cell Retargeting / Activation
- Others
Target Antigen
- C5-Albumin
- CD20 x CD3
- CD3 x BCMA
- CD3 x CD19
- EGFR x cMET
- EpCAM x CD3
- Factor IXa x Factor X
- gp100 x CD3
- HER2 x HER2
- PD-1 x CTLA-4
- PD-L1 x TGFB
- TNF-a x HSA
- VEGF x DLL4
- VEGF-A x ANG2
Antibody Format
- Asymmetric
- Fragments
Geography
- North America (US, Canada, Rest of North America)
- Europe (Germany, France, Italy, Spain, UK, Rest of Europe)
- Asia (India, China, Japan, South Korea, Rest of Asia)
- Rest of the World
Bispecific Antibodies Market: Growth and Trends
Assessing the therapeutic capabilities of monoclonal antibodies and their effective application in treating numerous diseases has transformed the pharmaceutical sector. Currently, extensive studies are underway to develop engineered antibody therapeutics to enhance treatment outcomes. Several decades ago, bispecific antibodies were developed by adding additional antigen binding sites to monoclonal antibodies. The primary goal of these bivalent molecules has been to guide cytotoxic immune effector cells to enhance the destruction of tumor cells through antibody-dependent cell-mediated cytotoxicity (ADCC) and various other cytotoxic processes driven by the immune effector cells. This modified version of antibody-based treatments is presently attracting significant interest from pharmaceutical firms. In recent years, clinical trials have shown significant advantages provided by innovative bispecific antibody treatments for various target conditions, creating substantial opportunities for those involved in developing these therapies.
The bispecific antibodies market is driven by major factors including the growing cancer burden, along with an increasing focus on personalized medicine for blood cancers, autoimmune diseases, and other such disorders. The rising financial burden of chronic diseases, along with its impact on death rates, has resulted in a heightened need for efficient bispecific antibody therapies that can address various oncological and non-oncological conditions. Consequently, R&D initiatives from both industry and non-industry entities, along with the increasing need for efficient bispecific antibody treatments, are expected to drive the bispecific antibodies market in the coming decade.
Bispecific Antibodies Market: Key Insights
The report delves into the current state of the bispecific antibodies market and identifies potential growth opportunities within the industry. Some key findings from the report include:
- The landscape of bispecific antibody therapeutics has steadily evolved in the past decade; over 400 clinical / preclinical candidates are being evaluated by over 120 drug developers worldwide.
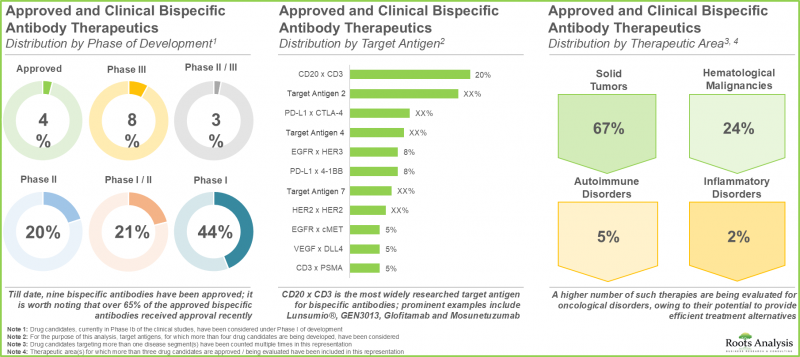
- The current pipeline features a number of clinical stage bispecific antibody drug candidates, capable of targeting a range of biological antigens in order to potentially treat multiple target indications.
- In fact, industry stakeholders are engaged in the development of over 85 bispecific antibody technology platforms, aiming to mitigate the existing manufacturing challenges associated with such therapies.
- The growing interest is evident from the rise in partnership activity; companies are actively entering into strategic agreements in order to expand their bispecific antibody portfolio.
- Since 2010, nearly 280 clinical trials have been registered to evaluate the safety and efficacy of various bispecific antibody therapeutics; majority of these studies are being conducted across sites in the US.
- In order to efficiently promote these therapies, drug developers are actively exploring diverse promotional strategies with an aim to sustain their position in the market.
- With the growing focus on development pipeline and encouraging clinical results, the market is expected to witness an annualized growth rate of over 6.5%, during the next decade.
Bispecific Antibodies Market: Key Segments
Hematological Malignancies is the Fastest Growing Segment of Bispecific Antibodies Market
In terms of therapeutic area, the market is segmented into autoimmune disorders, genetic disorders, hematological malignancies, ophthalmic disorders, skin cancers and solid tumors. At present, genetic disorders hold the maximum share of the bispecific antibodies market. It is worth highlighting that the bispecific antibodies market for hematological malignancies is likely to grow at a relatively higher CAGR.
Bispecific Antibodies Acting Through T-Cell Retargeting / Activation Occupy the Largest Share During the Forecast Period
In terms of mechanism of action, the market is segmented into cytokines retargeting / neutralization, dual ligands blocking, resistance factors co-targeting, targeting tumor angiogenesis, T-cell retargeting / activation and others. Currently, T-cell retargeting / activation holds the maximum share of the bispecific antibodies market. However, bispecific antibodies acting through cytokines retargeting / neutralization are anticipated to capture the highest market in the near future.
Bispecific Antibodies Targeting CD3 x BCMA is the Fastest Growing Segment of the Market
In terms of target antigen, the market is segmented into C5-Albumin,CD20 x CD3, CD3 x BCMA, CD3 x CD19, EGFR x cMET, EpCAM x CD3, Factor IXa x Factor X, gp100 x CD3, HER2 x HER2, PD-1 x CTLA-4, PD-L1 x TGFB, TNF-a x HSA, VEGF x DLL4 and VEGF-A x ANG2. At present, therapies targeting factor IXa x factor X holds the maximum share of the bispecific antibodies market. It is worth highlighting that the drugs intended to target CD3 x BCMA are likely to grow at a relatively higher CAGR.
Asymmetric Bispecific Antibodies are Likely to Dominate the Market During the Forecast Period
In terms of antibody format, the market is segmented into asymmetric and fragments. Currently, asymmetric antibodies hold the maximum share of the bispecific antibodies market. This trend is unlikely to change in the foreseeable future.
North America Accounts for the Largest Share of the Market
In terms of key geographical regions, the market is segmented into North America, Europe, Asia-Pacific and rest of the world. We anticipate North America to capture the majority of the bispecific antibodies market. Further, it is worth highlighting that Europe is expected to grow at a higher CAGR over the coming years.
Example Players in the Bispecific Antibodies Market
- Akeso Biopharma
- Alexion
- Amgen
- Genmab
- Immunocore
- Janssen Research & Development
- Linton Pharm
- Merck
- OncXerna Therapeutics
- Pfizer
- Roche
- Taisho Pharmaceutical
- Zymeworks
Primary Research Overview
The opinions and insights presented in this study were influenced by discussions conducted with multiple stakeholders. The research report features detailed transcripts of interviews held with the following industry stakeholders:
- Senior Scientist, Company A
- Business Development Consultant, Company B
- Director (GMP Clinical Manufacturing), Company C
- Former Senior Director, Business Development, Company D
- Founder and Chief Scientific Officer and Chief Executive Officer, Company E
- PhD Student, Company F
Bispecific Antibodies Market: Research Coverage
- Market Sizing and Opportunity Analysis: The report features an in-depth analysis of the bispecific antibodies market, focusing on key market segments, including [A] therapeutic area, [B] mechanism of action, [C] target antigen, [D] antibody format and [E] Key geographical regions.
- Market Landscape 1: A comprehensive evaluation of bispecific antibodies that are either approved or being evaluated in different stages of clinical development, considering various parameters, such as [A] developer company, [B] phase of development, [C] target antigen, [D] type of therapy, [E] route of administration, [F] method of administration, [G] target indication, [H] therapeutic area, [I] disease segment, [J] year of establishment, [K] company size and [L] location of headquarter.
- Market Landscape 2: A comprehensive evaluation of bispecific antibodies that are currently being evaluated in preclinical studies, considering various parameters, such as [A] developer company, [B] stage of development, [C] target antigen, [D] therapeutic area, [E] disease segment, [F] year of establishment, [G] company size and [H] location of headquarters of the developer.
- Key Insights: A detailed analysis, encompassing the contemporary bispecific antibody therapeutics market trends, based on relevant parameters, such as [A] phase of development and route of administration, [B] phase of development and disease segment, and [C] phase of development and location of their headquarters. In addition, this chapter includes various representations of preclinical stage bispecific antibody therapeutics based on [D] stage of development and disease segment, and [E] stage of development and location of their headquarters. Further, the chapter also includes representation of the developers of bispecific antibody therapeutics based on [F] stage of development (preclinical, clinical and preclinical and clinical) of their drug candidates and [G] location of their headquarters.
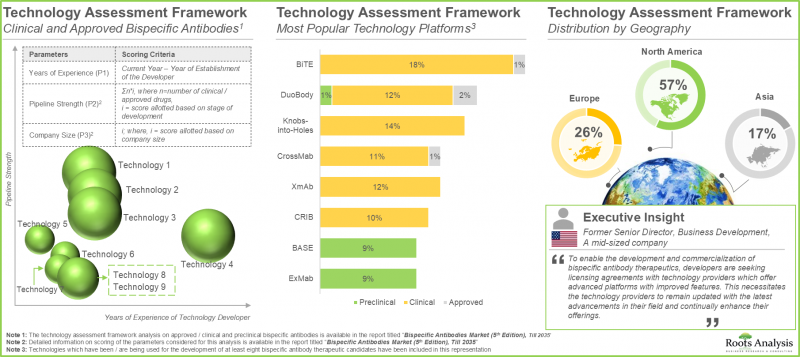
- Technology Assessment Framework: A detailed assessment of technology platforms being developed / used by various drug developers for the production of bispecific antibody therapeutics, based on multiple relevant parameters, such as [A] clinical / preclinical pipeline strength, [B] developer's years of experience, [C] company size and [D] location of headquarters of developers.
- Big Pharma Analysis: A comprehensive examination of various initiatives focused on bispecific antibody therapeutics undertaken by major pharmaceutical companies. This analysis includes heat map visualizations that illustrate the distribution of leading pharmaceutical firms, as well as spider web diagrams that compare their initiatives across multiple relevant parameters.
- Company Profiles: In-depth profiles of key industry players engaged in the development of bispecific antibodies across various geographies, focusing on [A] company overviews, [B] financial information (if available), [C] drug portfolio, [D] recent developments and [E] an informed future outlook.
- Partnerships and Collaborations: An analysis of partnerships established in this sector, since 2016, based on several parameters, such as [A] year of partnership, [B] type of partnership, [C] disease segment, [D] type of payment model employed, [E] deal amount, [F] most active players (in terms of number of deals inked), [G] most popular technologies (in terms of number of deals inked for technologies). This section also highlights the regional distribution of partnership activity in this market.
- Contract Services for Bispecific Antibody Therapeutics: A review on the key steps involved and challenges associated with the manufacturing of bispecific antibodies. In addition, this section includes a list of contract manufacturing organizations (CMOs) and biologics contract research organization (CROs), highlighting the key considerations for bispecific antibody developers, while selecting a suitable CRO / CMO.
- Clinical Trial Analysis: Examination of completed, ongoing, and planned clinical studies of various bispecific antibody therapeutics based on parameters like [A] trial registration year, [B] trial phase, [C] trial recruitment status, [D] enrolled patient population, [E] type of study, [F] study design, [G] type of sponsor / collaborator, [H] leading industry and non-industry players, [I] key focus areas and [J] geographical location of trials.
- Case Study 1: A discussion on general regulatory guidelines issued by the ICH, WHO and FDA for the development of bispecific antibodies. In addition, it provides details related to the responses of various pharmaceutical industries to the FDA guidelines.
- Case Study 2: A review of different channels used for promoting marketed bispecific antibodies, along with examples of players that have undertaken such initiatives, elaborating on the various promotional strategies being adopted by developers of two approved bispecific antibodies, namely Blincyto(R) and Hemlibra(R), and comparison of both the drugs based on information available on their respective websites.
- SWOT Analysis: A SWOT analysis, focusing on key drivers and challenges that are likely to impact the industry's evolution. Further, it includes a Harvey ball analysis, highlighting the relative effect of each SWOT parameter on the overall industry.
Key Questions Answered in this Report
- How many companies are currently engaged in this market?
- Which are the leading companies in this market?
- What kind of partnership models are commonly adopted by industry stakeholders?
- What are the factors that are likely to influence the evolution of this market?
- What is the current and future market size?
- What is the CAGR of this market?
- How is the current and future market opportunity likely to be distributed across key market segments?
Reasons to Buy this Report
- The report provides a comprehensive market analysis, offering detailed revenue projections of the overall market and its specific sub-segments. This information is valuable to both established market leaders and emerging entrants.
- Stakeholders can leverage the report to gain a deeper understanding of the competitive dynamics within the market. By analyzing the competitive landscape, businesses can make informed decisions to optimize their market positioning and develop effective go-to-market strategies.
- The report offers stakeholders a comprehensive overview of the market, including key drivers, barriers, opportunities, and challenges. This information empowers stakeholders to stay abreast of market trends and make data-driven decisions to capitalize on growth prospects.
Additional Benefits
- Complimentary PPT Insights Packs
- Complimentary Excel Data Packs for all Analytical Modules in the Report
- 15% Free Content Customization
- Detailed Report Walkthrough Session with Research Team
- Free Updated report if the report is 6-12 months old or older
TABLE OF CONTENTS
1. PREFACE
- 1.1. Introduction
- 1.2. Key Market Insights
- 1.3. Scope of the Report
- 1.4. Research Methodology
- 1.5. Frequently Asked Questions
- 1.6. Chapter Outlines
2. EXECUTIVE SUMMARY
3. INTRODUCTION
- 3.1. Chapter Overview
- 3.2. Introduction to Antibodies
- 3.2.1. Structure
- 3.2.2. Functions
- 3.2.3. Mechanism of Action
- 3.3. Antibody Therapeutics
- 3.3.1. Historical Evolution of Antibody Therapeutics
- 3.3.2. Key Approved Antibody Therapeutics
- 3.3.3. Advanced Antibody Therapeutics
- 3.3.3.1. Fc Engineered and Glycoengineered Antibodies
- 3.3.3.2. Antibody Fragments
- 3.3.3.3. Fusion Proteins
- 3.3.3.4. Intrabodies
- 3.3.3.5. Bispecific Antibodies
- 3.4. Bispecific Antibody Formats
- 3.4.1. Single-Chain-based Formats (Fc Independent Antibody Formats)
- 3.4.1.1. Tandem scFvs (single-chain variable fragments) and Triple bodies
- 3.4.1.2. Bispecific Single-Domain Antibody Fusion Proteins
- 3.4.1.3. Diabodies / Diabody Derivatives
- 3.4.1.4. Fusion Proteins
- 3.4.1.5. Fusion Proteins Devoid of Fc Regions
- 3.4.2. Immunoglobulin G Based Formats (Fc Dependent Antibody Formats)
- 3.4.2.1. Quadromas
- 3.4.2.2. Knobs-Into-Holes
- 3.4.2.3. Dual Variable Domain Ig
- 3.4.2.4. IgG-scFv
- 3.4.2.5. Two-in-one or Dual Action Fab (DAF) Antibodies
- 3.4.2.6. Half Molecule Exchange
- 3.4.2.7. κλ- Bodies
- 3.4.1. Single-Chain-based Formats (Fc Independent Antibody Formats)
- 3.5. Mechanism of Action of Bispecific Antibody Therapeutics
- 3.5.1. Retargeting Immune Effectors (NK Cells and T Cells) to Tumor Cells
- 3.5.2. Directly Targeting Malignant / Tumor Cells
- 3.5.3. Retargeting of Toxins
- 3.5.4. Targeting Tumor Angiogenesis
- 3.5.5. Other Mechanisms
- 3.6. Applications of Bispecific Antibodies
4. MARKET LANDSCAPE OF APPROVED AND CLINICAL THERAPIES
- 4.1. Chapter Overview
- 4.2. Approved and Clinical Bispecific Antibody Therapeutics: Overall Market Landscape
- 4.2.1. Analysis by Phase of Development
- 4.2.2. Analysis by Target Antigen
- 4.2.3. Analysis by Type of Therapy
- 4.2.4. Analysis by Route of Administration
- 4.2.5. Analysis by Method of Administration
- 4.2.6. Analysis by Target Indication
- 4.2.7. Analysis by Therapeutic Area
- 4.2.8. Analysis by Disease Segment
- 4.3. Approved and Clinical Bispecific Antibody Therapeutics: Overall Developer Landscape
- 4.3.1. Analysis by Year of Establishment
- 4.3.2. Analysis by Company Size
- 4.3.3. Analysis by Location of Headquarters
5. MARKET LANDSCAPE OF PRECLINICAL THERAPIES
- 5.1. Chapter Overview
- 5.2. Preclinical Bispecific Antibody Therapeutics: Overall Market Landscape
- 5.2.1. Analysis by Stage of Development
- 5.2.2. Analysis by Target Antigen
- 5.2.3. Analysis by Therapeutic Area and Disease Segment
- 5.3. Preclinical Bispecific Antibody Therapeutics: Overall Developer Landscape
- 5.3.1. Analysis by Year of Establishment
- 5.3.2. Analysis by Company Size
- 5.3.3. Analysis by Location of Headquarters
6. KEY INSIGHTS
- 6.1. Chapter Overview
- 6.2. Approved and Clinical Stage Bispecific Antibody Therapeutics Landscape: Key Insights
- 6.2.1. Analysis by Phase of Development and Route of Administration
- 6.2.2. Analysis by Phase of Development and Disease Segment
- 6.2.3. Analysis by Phase of Development and Location of Developer's Headquarters
- 6.3. Preclinical Stage Bispecific Antibody Therapeutics Landscape: Key Insights
- 6.3.1. Analysis by Stage of Development and Therapeutic Area
- 6.3.2. Analysis by Stage of Development and Location of Developer Headquarters
- 6.4. Bispecific Antibody Therapeutic Developers Landscape: Key Insights
- 6.4.1. Distribution by Stage of Development
- 6.4.2. Distribution by Stage of Development and Region of Developer Headquarters
7. TECHNOLOGY ASSESSMENT FRAMEWORK
- 7.1. Chapter Overview
- 7.2. Bispecific Antibody Therapeutics: List of Technology Platforms
- 7.3. Bispecific Antibody Technology Platforms: Comparative Analysis
- 7.3.1. Analysis by Technologies for Approved and Clinical Drugs
- 7.3.2. Analysis by Technologies for Preclinical Drugs
- 7.4. Most Popular Technology Platforms: Analysis by Stage of Development
- 7.5. Bispecific Antibody Technology Platform Developers: Analysis by Location of Headquarters
8. BIG PHARMA PLAYERS: BENCHMARKING ANALYSIS
- 8.1. Chapter Overview
- 8.2. Big Pharma Players: Benchmarking Analysis (Spider Web Representation)
- 8.3. Big Pharma Players: Comparative Clinical Pipeline Analysis
- 8.3.1. Analysis by Target Antigen
- 8.3.2. Analysis by Antibody Format
- 8.3.3. Analysis by Mechanism of Action
- 8.3.4. Analysis by Therapeutic Area
9. COMPANY PROFILES
- 9.1. Chapter Overview
- 9.2. Akeso Biopharma
- 9.2.1. Company Overview
- 9.2.2. Financial Performance
- 9.2.3. Drug Portfolio
- 9.2.4. Recent Developments and Future Outlook
- 9.3. Alphamab Oncology
- 9.3.1. Company Overview
- 9.3.2. Financial Performance
- 9.3.3. Drug Portfolio
- 9.3.4. Recent Developments and Future Outlook
- 9.4. Amgen
- 9.4.1. Company Overview
- 9.4.2. Financial Performance
- 9.4.3. Drug Portfolio
- 9.4.4. Recent Developments and Future Outlook
- 9.5. Merck
- 9.5.1. Company Overview
- 9.5.2. Financial Performance
- 9.5.3. Drug Portfolio
- 9.5.4. Recent Developments and Future Outlook
- 9.6. Regeneron
- 9.6.1. Company Overview
- 9.6.2. Financial Performance
- 9.6.3. Drug Portfolio
- 9.6.4. Recent Developments and Future Outlook
- 9.7. Roche
- 9.7.1. Company Overview
- 9.7.2. Financial Performance
- 9.7.3. Drug Portfolio
- 9.7.4. Recent Developments and Future Outlook
- 9.8. Xencor
- 9.8.1. Company Overview
- 9.8.2. Financial Performance
- 9.8.3. Drug Portfolio
- 9.8.4. Recent Developments and Future Outlook
10. PARTNERSHIPS AND COLLABORATIONS
- 10.1. Chapter Overview
- 10.2. Partnership Models
- 10.3. Bispecific Antibody Therapeutics: Partnerships and Collaborations
- 10.3.1. Analysis by Year of Partnership
- 10.3.2. Analysis by Type of Partnership
- 10.3.3. Analysis by Year and Type of Partnership
- 10.3.4. Analysis by Disease Segment
- 10.3.5. Analysis by Type of Payment Model Employed and Deal Amount
- 10.3.6. Analysis by Year of Agreement, Type of Payment Model Employed and Deal Amount
- 10.3.7. Analysis by Disease Segment, Type of Payment Model Employed and Deal Amount
- 10.3.8. Most Active Players: Analysis by Number of Partnership Instances
- 10.3.9. Most Popular Technologies: Analysis by Number of Partnership Instances
- 10.3.10. Analysis by Region
- 10.3.11. Intercontinental and Intracontinental Agreements
11. CONTRACT SERVICES FOR BISPECIFIC ANTIBODY THERAPEUTICS
- 11.1. Chapter Overview
- 11.2. Manufacturing of Bispecific Antibody Therapeutics
- 11.2.1. Key Considerations for Manufacturing and Associated Challenges
- 11.2.2. Contract Manufacturing Organizations (CMOs)
- 11.2.2.1. Bispecific Antibody Therapeutics: List of CMOs
- 11.2.3. Contract Research Organizations (CROs)
- 11.2.3.1. Bispecific Antibody Therapeutics: List of CROs
- 11.3. Key Considerations for Selecting a Suitable CMO / CRO Partner
12. CLINICAL TRIAL ANALYSIS
- 12.1. Chapter Overview
- 12.2. Key Assumptions and Methodology
- 12.3. Bispecific Antibody Therapeutics: Clinical Trial Analysis
- 12.3.1. Analysis by Trial Registration Year
- 12.3.2. Analysis of Enrolled Patient Population by Trial Registration Year
- 12.3.3. Analysis by Trial Phase
- 12.3.4. Analysis of Enrolled Patient Population by Trial Phase
- 12.3.5. Analysis by Trial Recruitment Status
- 12.3.6. Analysis by Trial Registration Year and Trial Recruitment Status
- 12.3.7. Analysis by Type of Study
- 12.3.8. Analysis by Study Design
- 12.3.9. Analysis by Type of Sponsor / Collaborator
- 12.3.10. Leading Industry Players: Analysis by Number of Registered Trials
- 12.3.11. Leading Non-Industry Players: Analysis by Number of Registered Trials
- 12.3.12. Clinical Trial Analysis: Key Focus Areas (Word Cloud Representation)
- 12.3.13. Analysis by Geography
- 12.3.14. Analysis by Trial Recruitment Status and Geography
- 12.3.15. Analysis of Enrolled Patient Population by Trial Recruitment Status and Geography
13. CASE STUDY: REGULATORY GUIDELINES FOR BISPECIFIC ANTIBODIES
- 13.1. Chapter Overview
- 13.2. Guidelines Issued by Regulatory Authorities
- 13.2.1. US Food and Drug Administration (FDA)
- 13.2.1.1. Pharma Companies' Response to the FDA Draft Guidance
- 13.2.2. World Health Organization (WHO)
- 13.2.1. US Food and Drug Administration (FDA)
14. CASE STUDY: PROMOTIONAL / MARKETING STRATEGIES
- 14.1. Chapter Overview
- 14.2. Key Channels Used for Promotional Campaigns
- 14.2.1. Product Websites
- 14.2.2. Patient Assistance Programs
- 14.2.3. Participation in Conferences
- 14.2.4. Collaboration with Stakeholders
- 14.2.5. Drug Approval Across Multiple Geographies
- 14.3. Other Channels Used for Promotional and Marketing Strategies
- 14.4. Summary: Promotional and Marketing Strategy Leveraged by Bispecific Antibody Developers
- 14.5. Promotional Analysis: Blincyto(R)
- 14.5.1. Drug Overview
- 14.5.2. Product Website analysis
- 14.5.2.1. Messages for Healthcare Professionals
- 14.5.2.1.1. For MRD Positive B-cell precursor ALL
- 14.5.2.1.2. For Relapsed or Refractory B-cell precursor ALL
- 14.5.2.2. Messages for Patients
- 14.5.2.1. Messages for Healthcare Professionals
- 14.5.3. Patient Support Services and Informative Downloads
- 14.5.4. Other Promotional Strategies
- 14.5.4.1. Presence in Conferences
- 14.6. Promotional Analysis: Hemlibra(R)
- 14.6.1. Drug Overview
- 14.6.2. Product Website Analysis
- 14.6.2.1. Messages for Healthcare Professionals
- 14.6.2.1.1. For Hemophilia A without Factor VIII Inhibitors
- 14.6.2.1.2. For Hemophilia A with Factor VIII Inhibitors
- 14.6.2.3. Messages for Patients
- 14.6.2.1. Messages for Healthcare Professionals
- 14.6.3. Patient Support Services and Informative Downloads
- 14.6.3.1. Co-pay Program
- 14.6.3.2. Independent Co-pay Assistance Foundation
- 14.6.3.3. Genentech Patient Foundation
- 14.6.4. Other Promotional Strategies
- 14.6.4.1. Presence in Conferences
15. MARKET FORECAST AND OPPORTUNITY ANALYSIS
- 15.1. Chapter Overview
- 15.2. Scope and Limitations
- 15.3. Forecast Methodology and Key Assumptions
- 15.4. Bispecific Antibody Therapeutics Market, till 2035
- 15.4.1. Bispecific Antibody Therapeutics Market: Analysis by Therapeutic Area, Current Year and 2035
- 15.4.2. Bispecific Antibody Therapeutics Market: Analysis by Mechanism of Action, Current Year and 2035
- 15.4.3. Bispecific Antibody Therapeutics Market: Analysis by Target Antigen, Current Year and 2035
- 15.4.4. Bispecific Antibody Therapeutics Market: Analysis by Antibody Format, Current Year and 2035
- 15.4.5. Bispecific Antibody Therapeutics Market: Analysis by Key Players, Current Year and 2035
- 15.4.6. Bispecific Antibody Therapeutics Market: Analysis by Geography, Current Year and 2035
- 15.5. Bispecific Antibody Market: Value Creation Analysis
- 15.6. Bispecific Antibody Therapeutics Market: Product-wise Sales Forecasts
- 15.6.1. AK104 (Akeso Biopharma)
- 15.6.1.1. Target Patient Population
- 15.6.1.2. Sales Forecast
- 15.6.1.3. Net Present Value
- 15.6.1.4. Value Creation Analysis
- 15.6.2. Blincyto(TM) (Amgen)
- 15.6.2.1. Target Patient Population
- 15.6.2.2. Sales Forecast
- 15.6.2.3. Net Present Value
- 15.6.2.4. Value Creation Analysis
- 15.6.3. Hemlibra(R) (Roche)
- 15.6.3.1. Target Patient Population
- 15.6.3.2. Sales Forecast
- 15.6.3.3. Net Present Value
- 15.6.3.4. Value Creation Analysis
- 15.6.4. Kimmtrak(R) (Immunocore)
- 15.6.4.1. Target Patient Population
- 15.6.4.2. Sales Forecast
- 15.6.4.3. Net Present Value
- 15.6.4.4. Value Creation Analysis
- 15.6.5. Lunsumio(R) (Roche)
- 15.6.5.1. Target Patient Population
- 15.6.5.2. Sales Forecast
- 15.6.5.3. Net Present Value
- 15.6.5.4. Value Creation Analysis
- 15.6.6. Nanozora(R) (Taisho Pharmaceutical)
- 15.6.6.1. Target Patient Population
- 15.6.6.2. Sales Forecast
- 15.6.6.3. Net Present Value
- 15.6.6.4. Value Creation Analysis
- 15.6.7. Rybrevant(TM) (Janssen Research & Development)
- 15.6.7.1. Target patient Population
- 15.6.7.2. Sales Forecast
- 15.6.7.3. Net Present Value
- 15.6.7.4. Value Creation Analysis
- 15.6.8. Tecvayli(TM) (Janssen Research & Development)
- 15.6.8.1. Target Patient Population
- 15.6.8.2. Sales Forecast
- 15.6.8.3. Net Present Value
- 15.6.8.4. Value Creation Analysis
- 15.6.9. Vabysmo(TM) (Roche)
- 15.6.9.1. Target Patient Population
- 15.6.9.2. Sales Forecast
- 15.6.9.3. Net Present Value
- 15.6.9.4. Value Creation Analysis
- 15.6.10. AK112 (Akeso Biopharma)
- 15.6.10.1. Target Patient Population
- 15.6.10.2. Sales Forecast
- 15.6.10.3. Net Present Value
- 15.6.10.4. Value Creation Analysis
- 15.6.11. ALXN1720 (Alexion)
- 15.6.11.1. Target Patient Population
- 15.6.11.2. Sales Forecast
- 15.6.11.3. Net Present Value
- 15.6.11.4. Value Creation Analysis
- 15.6.12. GEN3013 (Genmab)
- 15.6.12.1. Target Patient Population
- 15.6.12.2. Sales Forecast
- 15.6.12.3. Net Present Value
- 15.6.12.4. Value Creation Analysis
- 15.6.13. Glofitamab (Roche)
- 15.6.13.1. Target Patient Population
- 15.6.13.2. Sales Forecast
- 15.6.13.3. Net Present Value
- 15.6.13.4. Value Creation Analysis
- 15.6.14. LP000 (Linton Pharm)
- 15.6.14.1. Target Patient Population
- 15.6.14.2. Sales Forecast
- 15.6.14.3. Net Present Value
- 15.6.14.4. Value Creation Analysis
- 15.6.15. M7824 (Merck)
- 15.6.15.1. Target Patient Population
- 15.6.15.2. Sales Forecast
- 15.6.15.3. Net Present Value
- 15.6.15.4. Value Creation Analysis
- 15.6.16. OMP 305B83 (Mereo BioPharma)
- 15.6.16.1. Target Patient Population
- 15.6.16.2. Sales Forecast
- 15.6.16.3. Net Present Value
- 15.6.16.4. Value Creation Analysis
- 15.6.17. PF-06863135 (Pfizer)
- 15.6.17.1. Target Patient Population
- 15.6.17.2. Sales Forecast
- 15.6.17.3. Net Present Value
- 15.6.17.4. Value Creation Analysis
- 15.6.18. ZW25 (Zymeworks)
- 15.6.18.1. Target Patient Population
- 15.6.18.2. Sales Forecast
- 15.6.18.3. Net Present Value
- 15.6.18.4. Value Creation Analysis
- 15.6.1. AK104 (Akeso Biopharma)
- 15.7. Concluding Remarks
16. SWOT ANALYSIS
- 16.1. Chapter Overview
- 16.2. Strengths
- 16.2.1. Enhanced Specificity
- 16.2.2. Diverse Application Areas
- 16.2.3. Lower Drug Resistance
- 16.2.4. Success of Approved Products
- 16.3. Weaknesses
- 16.3.1. Uncertainties with Safety of Therapeutic Candidates
- 16.3.2. Complex Purification and Downstream Processing
- 16.3.3. Dimerization in Antibodies with Fc-region
- 16.4. Opportunities
- 16.4.1. Life Cycle Management of Novel Therapies
- 16.4.2. Growing Number of High Value Partnerships
- 16.4.3. Expertise Available with Contract Manufacturing Organizations
- 16.4.4. Emergence of Advanced Technologies
- 16.5. Threats
- 16.5.1. Rise in Attrition Rate of Clinical Stage Candidates
- 16.6. Concluding Remarks
17. CONCLUDING REMARKS
18. EXECUTIVE INSIGHTS
- 18.1. Chapter Overview
- 18.2. Company A
- 18.2.1. Company Snapshot
- 18.2.2. Interview Transcript: Senior Scientist
- 18.3. Company B
- 18.3.1. Company Snapshot
- 18.3.2. Interview Transcript: PhD Student
- 18.4. Company C
- 18.4.1. Company Snapshot
- 18.4.2. Interview Transcript: Founder and Chief Scientific Officer, and Chief Executive Officer
- 18.5. Company D
- 18.5.1. Company Snapshot
- 18.5.2. Interview Transcript: Former Senior Director, Business Development
- 18.6. Company E
- 18.6.1. Company Snapshot
- 18.6.2. Interview Transcript: Business Development Consultant
- 18.7. Company F
- 18.7.1. Company Snapshot
- 18.7.2. Interview Transcript: Director, GMP Clinical Manufacturing





